Tänapäeval on alkoholivaba rasvmaks (NAFLD) saanud peamiseks kroonilise maksahaiguse põhjuseks Hiinas ja isegi kogu maailmas. Haiguste spekter hõlmab lihtsat maksa steatohepatiiti, alkoholivaba steatohepatiiti (NASH) ning sellega seotud tsirroosi ja maksavähki. NASH-i iseloomustab liigne rasva kogunemine hepatotsüütidesse ning indutseeritud rakukahjustus ja põletik, koos maksafibroosiga või ilma. Maksafibroosi raskusaste NASH-i patsientidel on tihedalt seotud halva maksaprognoosiga (tsirroos ja selle tüsistused ning hepatotsellulaarne kartsinoom), kardiovaskulaarsete sündmuste, ekstrahepaatiliste pahaloomuliste kasvajate ja surmaga mis tahes põhjusel. NASH võib patsientide elukvaliteeti negatiivselt mõjutada; aga NASH-i raviks ei ole heaks kiidetud ühtegi ravimit ega ravi.
Hiljuti ajakirjas New England Journal of Medicine (NEJM) avaldatud uuring (ENLIVEN) näitas, et pegosafermiin parandas nii maksafibroosi kui ka maksapõletikku biopsiaga kinnitatud tsirroosita NASH-patsientidel.
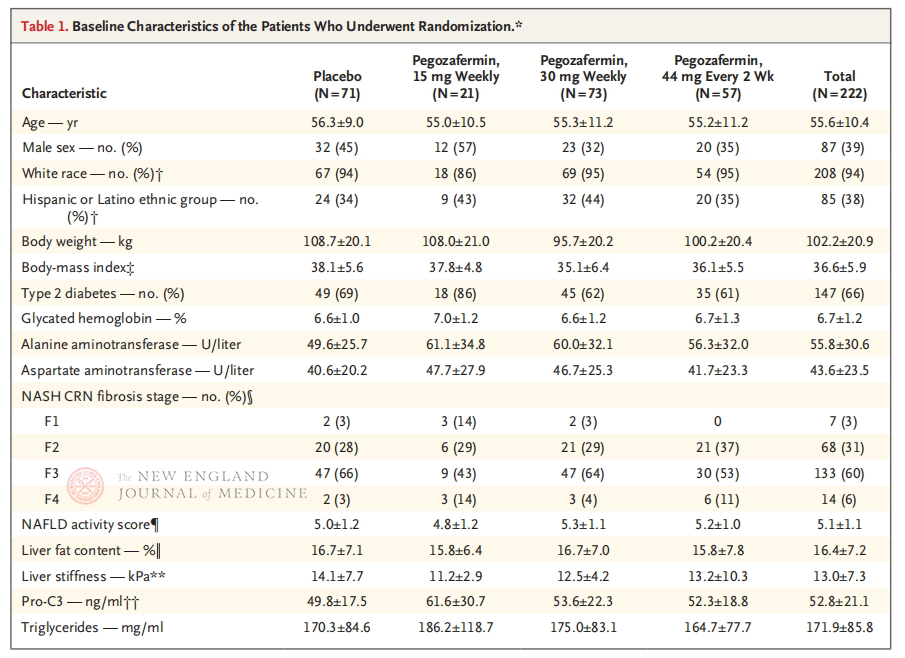
Mitmekeskuseline, randomiseeritud, topeltpime, platseebokontrolliga IIb faasi kliiniline uuring, mille viisid läbi professor Rohit Loomba ja tema kliiniline meeskond California Ülikooli San Diego Meditsiinikoolis, kaasas 222 patsienti, kellel oli biopsiaga kinnitatud F2-3 staadiumi NASH ajavahemikus 28. september 2021 kuni 15. august 2022. Patsientidele manustati juhuslikult pegosafermiini (subkutaanne süst, 15 mg või 30 mg üks kord nädalas või 44 mg üks kord iga 2 nädala järel) või platseebot (üks kord nädalas või üks kord iga 2 nädala järel). Esmased tulemusnäitajad olid fibroosi ≥ 1. staadiumi paranemine ja NASH-i progresseerumise puudumine. NASH taandus ilma fibroosse progresseerumiseta. Uuringus viidi läbi ka ohutushindamine.
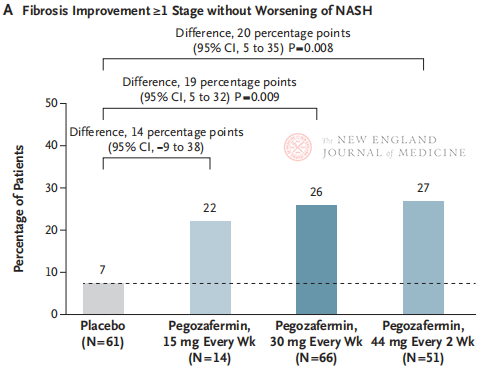
Pärast 24-nädalast ravi oli patsientide osakaal, kellel esines ≥ 1. staadiumi fibroosi paranemine ja NASH-i süvenemise puudumine, ning patsientide osakaal, kellel esines NASH-i regressioon ja fibroosi süvenemise puudumine, Pegozafermiini kolmes annustamisrühmas oluliselt suurem kui platseeborühmas, kusjuures olulisemad erinevused esinesid patsientidel, keda raviti 44 mg üks kord iga kahe nädala tagant või 30 mg üks kord nädalas. Ohutuse osas oli pegozafermiin sarnane platseeboga. Pegozafermiinraviga seotud kõige sagedasemad kõrvaltoimed olid iiveldus, kõhulahtisus ja süstekoha erüteem. Käesolevas IIb faasi uuringus näitavad esialgsed tulemused, et ravi pegozafermiiniga parandab maksafibroosi.
Selles uuringus kasutatud pegozafermiin on inimese fibroblastide kasvufaktori 21 (FGF21) pika toimeajaga glükoleeritud analoog. FGF21 on maksa poolt eritatav endogeenne metaboolne hormoon, millel on roll lipiidide ja glükoosi metabolismi reguleerimisel. Varasemad uuringud on näidanud, et FGF21-l on NASH-i patsientidele terapeutiline toime, suurendades maksa insuliinitundlikkust, stimuleerides rasvhapete oksüdatsiooni ja pärssides lipogeneesi. Loodusliku FGF21 lühike poolväärtusaeg (umbes 2 tundi) piirab aga selle kasutamist NASH-i kliinilises ravis. Pegozafermiin kasutab glükosüülitud pegüleerimise tehnoloogiat, et pikendada loodusliku FGF21 poolväärtusaega ja optimeerida selle bioloogilist aktiivsust.
Lisaks selle IIb faasi kliinilise uuringu positiivsetele tulemustele näitas hiljuti ajakirjas Nature Medicine avaldatud uuring (ENTRIGUE), et pegosafermiin vähendas oluliselt ka triglütseriidide, mitte-HDL-kolesterooli, apolipoproteiin B ja maksa steatoosi taset raske hüpertriglütserideemiaga patsientidel, millel võib olla positiivne mõju kardiovaskulaarsete sündmuste riski vähendamisele NASH-iga patsientidel.
Need uuringud näitavad, et pegozafermiin kui endogeenne metaboolne hormoon võib pakkuda NASH-iga patsientidele mitmeid metaboolseid eeliseid, eriti kuna NASH-i võidakse tulevikus ümber nimetada metaboolselt seotud rasvmaksaks. Need tulemused muudavad selle NASH-i ravis väga oluliseks potentsiaalseks ravimiks. Samal ajal toetavad need positiivsed uuringutulemused pegozafermiini kaasamist 3. faasi kliinilistesse uuringutesse.
Kuigi nii iga kahe nädala tagant manustatav 44 mg pegozafermiinravi kui ka iganädalane 30 mg manustamine saavutasid uuringu histoloogilise esmase tulemusnäitaja, oli ravi kestus selles uuringus vaid 24 nädalat ja platseeborühmas oli ravijärgimise määr vaid 7%, mis oli oluliselt madalam kui varasemate 48 nädalat kestnud kliiniliste uuringute tulemused. Kas erinevused ja turvalisus on samad? Arvestades NASH-i heterogeensust, on tulevikus vaja suuremaid, mitmekeskuselisi, rahvusvahelisi kliinilisi uuringuid, mis hõlmaksid suuremaid patsientide populatsioone ja pikendaksid ravi kestust, et paremini hinnata ravimi efektiivsust ja ohutust.
Postituse aeg: 16. september 2023