Epilepsiaga fertiilses eas naiste puhul on krambivastaste ravimite ohutus kriitilise tähtsusega nii nende endi kui ka nende järglaste jaoks, kuna raseduse ja imetamise ajal on krampide mõju vähendamiseks sageli vaja ravimeid. Probleemiks on see, kas ema epilepsiavastane ravi raseduse ajal mõjutab loote organite arengut. Varasemad uuringud on näidanud, et traditsiooniliste krambivastaste ravimite hulgas võivad valproehape, fenobarbitaal ja karbamasepiin kujutada endast teratogeenset riski. Uute krambivastaste ravimite hulgas peetakse lamotrigiini lootele suhteliselt ohutuks, samas kui topiramaat võib suurendada loote huule- ja suulaelõhe riski.
Mitmed neuroloogilise arengu uuringud on näidanud seost ema poolt raseduse ajal kasutatava valproehappe ja järglaste kognitiivse funktsiooni languse, autismi ja tähelepanupuudulikkuse ja hüperaktiivsuse häire (ADHD) vahel. Siiski on kvaliteetsed tõendid ema poolt raseduse ajal kasutatava topiramaadi ja järglaste neuroloogilise arengu vahelise seose kohta endiselt ebapiisavad. Õnneks avaldati eelmisel nädalal ajakirjas New England Journal of Medicine (NEJM) uus uuring veelgi rohkem tõendeid.
Reaalses maailmas ei ole epilepsiaga rasedate naiste puhul, kes vajavad krambivastaseid ravimeid, võimalik läbi viia ulatuslikke randomiseeritud kontrollitud uuringuid, et uurida ravimite ohutust. Seetõttu on rasedusregistrid, kohortuuringud ja juhtumikontrolli uuringud muutunud sagedamini kasutatavateks uuringu ülesehitusteks. Metodoloogilisest vaatenurgast on see uuring üks kvaliteetsemaid uuringuid, mida praegu saab rakendada. Selle olulisemad punktid on järgmised: kasutatakse populatsioonipõhist suure valimiga kohortuuringu meetodit. Kuigi ülesehitus on retrospektiivne, pärinevad andmed kahest suurest riiklikust andmebaasist USA Medicaidi ja Medicare'i süsteemides, mis on varem kaasatud, seega on andmete usaldusväärsus kõrge; keskmine jälgimisaeg oli 2 aastat, mis vastas põhimõtteliselt autismi diagnoosimiseks vajalikule ajale, ja ligi 10% (kokku üle 400 000 juhtumi) jälgiti kauem kui 8 aastat.
Uuringus osales üle 4 miljoni raseda naise, kellest 28 952-l diagnoositi epilepsia. Naised rühmitati vastavalt sellele, kas nad võtsid epilepsiavastaseid ravimeid või erinevaid epilepsiavastaseid ravimeid pärast 19. rasedusnädalat (staadium, mil sünapsid jätkavad moodustumist). Topiramaat oli ravimit saanud rühmas, valproehape positiivses kontrollrühmas ja lamotrigiin negatiivses kontrollrühmas. Ravimit mitte saanud kontrollrühma kuulusid kõik rasedad naised, kes ei võtnud mingeid krambivastaseid ravimeid 90 päevast enne viimast menstruatsiooni kuni sünnituseni (sh mitteaktiivne või ravimata epilepsia).
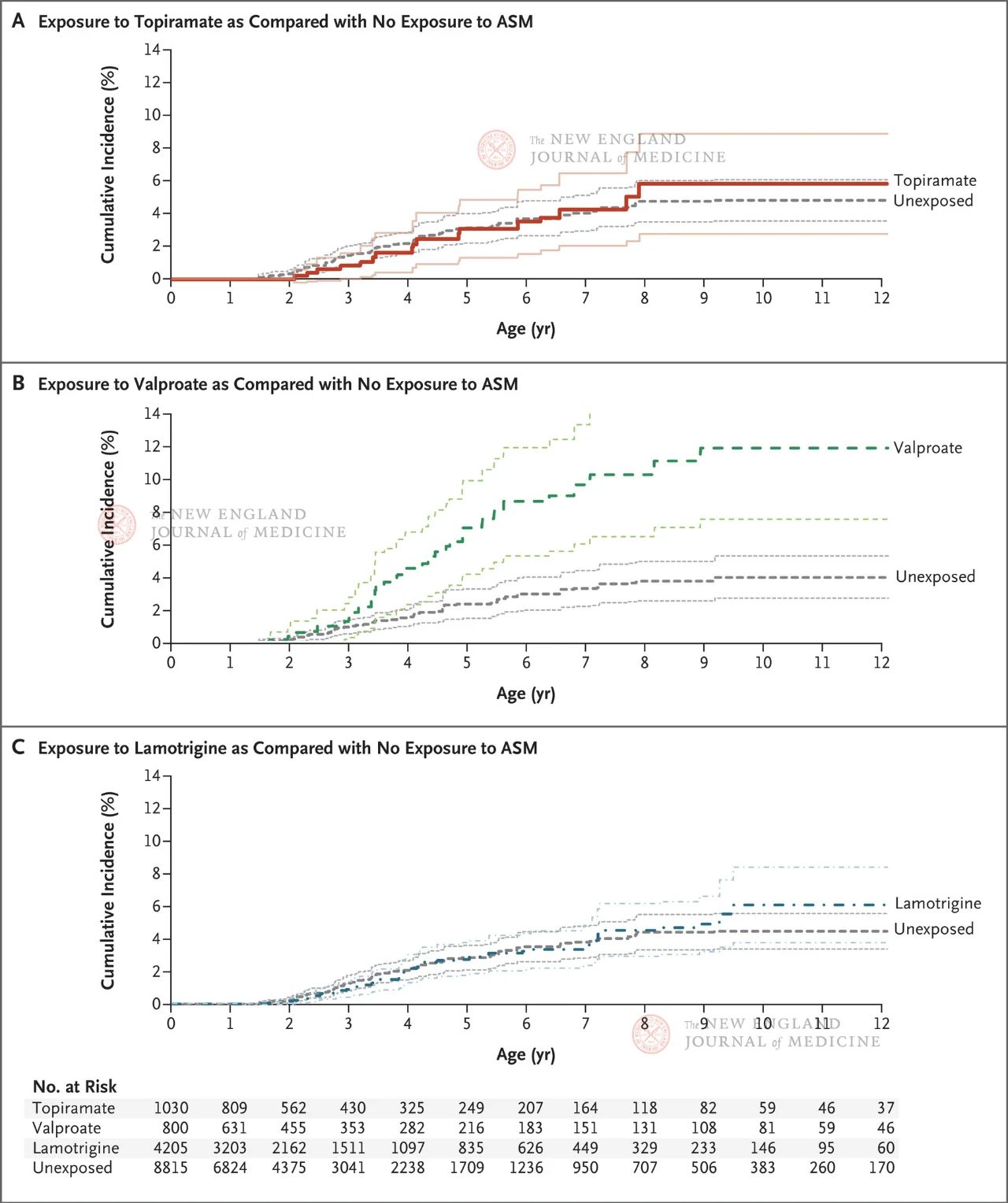
Tulemused näitasid, et hinnanguline autismi kumulatiivne esinemissagedus 8-aastaselt oli 1,89% kõigi järglaste seas, kes ei olnud kokku puutunud ühegi epilepsiavastase ravimiga; Epilepsiaga emade järglaste seas oli autismi kumulatiivne esinemissagedus 4,21% (95% CI, 3,27–5,16) lastel, kes ei olnud kokku puutunud epilepsiavastaste ravimitega. Topiramaadi, valproaadi või lamotrigiini saanud järglaste autismi kumulatiivne esinemissagedus oli vastavalt 6,15% (95% CI, 2,98–9,13), 10,51% (95% CI, 6,78–14,24) ja 4,08% (95% CI, 2,75–5,41).
Võrreldes loodetega, kes ei olnud krambivastaste ravimitega kokku puutunud, oli kalduvusskoori suhtes korrigeeritud autismi risk järgmine: topiramaadi rühmas oli see 0,96 (95% CI, 0,56–1,65), valproehappe rühmas 2,67 (95% CI, 1,69–4,20) ja lamotrigiini rühmas 1,00 (95% CI, 0,69–1,46). Alarühma analüüsis jõudsid autorid sarnastele järeldustele, lähtudes sellest, kas patsiendid said monoteraapiat, ravimi annusest ja sellest, kas raseduse alguses esines sellega seotud ravimiekspositsioon.
Tulemused näitasid, et epilepsiaga rasedate naiste järglastel oli suurem autismi risk (4,21 protsenti). Ei topiramaat ega lamotrigiin suurendanud autismi riski emade järglastel, kes võtsid raseduse ajal krambivastaseid ravimeid; valproehappe võtmisel raseduse ajal oli aga järglastel annusest sõltuv autismi riski suurenemine. Kuigi uuring keskendus ainult autismi esinemissagedusele rasedate naiste järglastel, kes võtsid krambivastaseid ravimeid, ega hõlmanud muid levinud neuroloogilise arengu tulemusi, nagu järglaste kognitiivne langus ja ADHD, peegeldab see siiski topiramaadi suhteliselt nõrka neurotoksilisust järglastel võrreldes valproaadiga.
Topiramaati ei peeta üldiselt naatriumvalproaadi soodsaks asendajaks raseduse ajal, kuna see võib suurendada huule- ja suulaelõhe ning raseduseaja kohta väikese sünnikaalu riski. Lisaks on uuringuid, mis viitavad sellele, et topiramaat võib suurendada järglaste neuroloogilise arengu häirete riski. NEJM-i uuring näitab aga, et kui arvestada ainult mõju järglaste neuroloogilisele arengule, siis rasedate naiste puhul, kes peavad kasutama valproaati epilepsiavastaste krampide raviks, on vajalik suurendada järglaste neuroloogilise arengu häirete riski. Topiramaati saab kasutada alternatiivse ravimina. Tuleb märkida, et Aasia ja teiste Vaikse ookeani saarte elanike osakaal kogu kohordis on väga madal, moodustades vaid 1% kogu kohordist, ning krambivastaste ravimite kõrvaltoimetes võib esineda rassilisi erinevusi, seega tuleb tulevikus kinnitada, kas selle uuringu tulemusi saab otseselt laiendada Aasia inimestele (sealhulgas Hiina inimestele).
Postituse aeg: 30. märts 2024