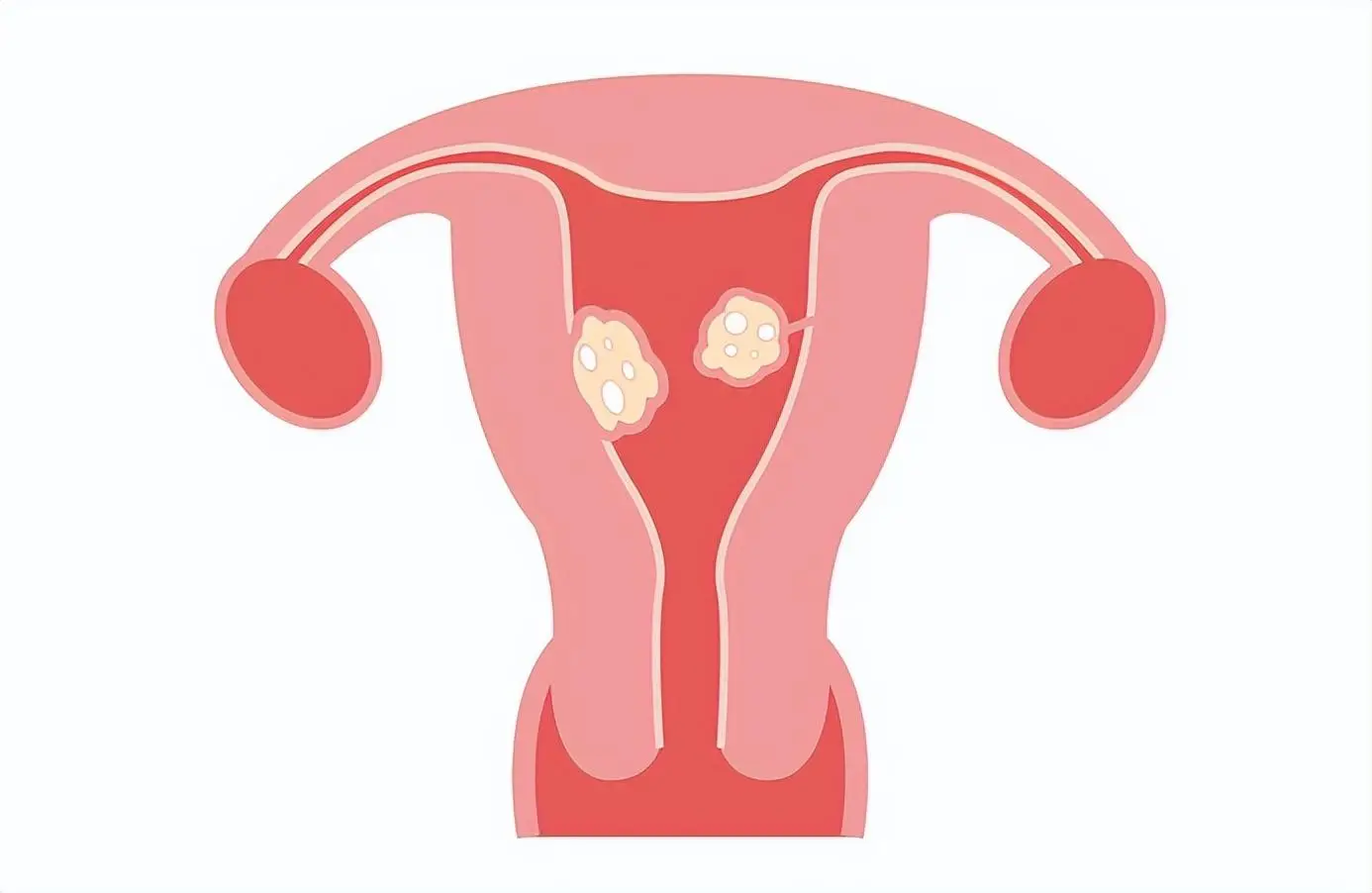
Emakafibroidid on menorraagia ja aneemia sagedane põhjus ning esinemissagedus on äärmiselt kõrge, umbes 70–80%-l naistest tekivad elu jooksul emakafibroidid, millest 50%-l ilmnevad sümptomid. Praegu on hüsterektoomia kõige sagedamini kasutatav ravi ja seda peetakse fibroidide radikaalseks raviks, kuid hüsterektoomiaga kaasnevad lisaks perioperatiivsetele riskidele ka suurenenud pikaajaline südame-veresoonkonna haiguste, ärevuse, depressiooni ja surma risk. Seevastu sellised ravivõimalused nagu emakaarteri emboliseerimine, lokaalne ablatsioon ja suukaudsed GnRH antagonistid on ohutumad, kuid neid ei kasutata täielikult ära.
Juhtumi kokkuvõte
33-aastane mustanahaline naine, kes polnud kunagi rase olnud, pöördus oma perearsti poole tugeva menstruatsiooni ja kõhugaasidega. Ta põeb rauavaegusaneemiat. Talasseemia ja sirprakulise aneemia testid olid negatiivsed. Patsiendi väljaheites ei olnud verd ning perekonnas ei olnud esinenud käärsoolevähki ega põletikulist soolehaigust. Ta teatas regulaarsest menstruatsioonist, üks kord kuus, iga 8-päevane periood, ja pikaajaliselt muutumatuna. Iga menstruaaltsükli kolmel kõige viljakamal päeval peab ta kasutama 8–9 tampooni päevas ja aeg-ajalt esineb menstruaalverejooksu. Ta õpib doktorantuuris ja plaanib kahe aasta jooksul rasestuda. Ultraheli näitas suurenenud emakat mitmete müoomide ja normaalsete munasarjadega. Kuidas te patsienti ravite?
Emakafibroididega seotud haiguste esinemissagedust süvendab haiguse madal avastamismäär ja asjaolu, et selle sümptomeid seostatakse muude seisunditega, näiteks seedehäirete või vereringehäiretega. Menstruatsioonist rääkimisega kaasnev häbi paneb paljud pika või vererohke menstruatsiooniga inimesed teadmatust oma seisundi ebanormaalsusest. Sümptomitega inimestel ei diagnoosita haigust sageli õigeaegselt. Kolmandikul patsientidest kulub diagnoosi saamiseks viis aastat ja mõnel rohkem kui kaheksa aastat. Hilinenud diagnoos võib negatiivselt mõjutada viljakust, elukvaliteeti ja rahalist heaolu ning kvalitatiivses uuringus teatas 95 protsenti sümptomaatiliste fibroididega patsientidest psühholoogilistest järelmõjudest, sealhulgas depressioonist, murest, vihast ja kehapildi halvatusest. Menstruatsiooniga seotud häbimärgistamine ja häbi takistavad selles valdkonnas arutelu, uurimistööd, propageerimist ja innovatsiooni. Ultraheli abil fibroididega diagnoositud patsientidest ei olnud 50–72% varem teadlikud, et neil on fibroidid, mis viitab sellele, et ultraheli võidakse selle levinud haiguse hindamisel laialdasemalt kasutada.
Emakafibroidide esinemissagedus suureneb vanusega kuni menopausini ja on mustanahalistel suurem kui valgetel. Võrreldes teiste inimestega tekivad mustanahalistel emakafibroidid nooremas eas, neil on suurem sümptomite tekke kumulatiivne risk ja suurem üldine haiguskoormus. Võrreldes valgetega on mustanahalised haigemad ja neil tehakse suurema tõenäosusega hüsterektoomia ja müomektoomia. Lisaks valisid mustanahalised valgetest tõenäolisemalt mitteinvasiivse ravi ja vältisid kirurgilist suunamist, et vältida hüsterektoomia võimalust.
Emaka fibroidid saab diagnoosida otse vaagna ultraheli abil, kuid sõeluuringu läbiviija kindlaksmääramine pole lihtne ja praegu tehakse sõeluuring tavaliselt pärast seda, kui patsiendi fibroidid on suured või ilmnevad sümptomid. Emaka fibroididega seotud sümptomid võivad kattuda ovulatsioonihäirete, adenomüopaatia, sekundaarse düsmenorröa ja seedehäirete sümptomitega.
Kuna nii sarkoomid kui ka fibroidid avalduvad müomeetriliste massidena ja nendega kaasneb sageli ebanormaalne emakaverejooks, on mure, et emakasarkoomid võivad vaatamata nende suhtelisele haruldusele (1 juhtum 770–10 000 visiidil ebanormaalse emakaverejooksu tõttu) jääda märkamata. Mure diagnoosimata leiomüosarkoomi pärast on viinud hüsterektoomia esinemissageduse suurenemiseni ja minimaalselt invasiivsete protseduuride kasutamise vähenemiseni, pannes patsiendid ebavajalikku tüsistuste ohtu emakast väljapoole levinud emakasarkoomide halva prognoosi tõttu.
Diagnoos ja hindamine
Emaka fibroidide diagnoosimiseks kasutatavatest erinevatest pildistamismeetoditest on vaagna ultraheli kõige kulutõhusam meetod, kuna see annab teavet emaka fibroidide mahu, asukoha ja arvu kohta ning aitab välistada manusmasse. Ambulatoorset vaagna ultraheli saab kasutada ka ebanormaalse emakaverejooksu, uuringu ajal palpeeritava vaagnamassi ja emaka suurenemisega seotud sümptomite, sealhulgas vaagna rõhu ja kõhugaaside hindamiseks. Kui emaka maht ületab 375 ml või fibroidide arv ületab 4 (mis on tavaline), on ultraheli eraldusvõime piiratud. Magnetresonantstomograafia on väga kasulik emaka sarkoomi kahtluse korral ja hüsterektoomia alternatiivi planeerimisel, mille puhul on ravitulemuste seisukohalt oluline täpne teave emaka mahu, pildistamisfunktsioonide ja asukoha kohta (joonis 1). Kui kahtlustatakse submukosaalseid fibroide või muid endomeetriumi kahjustusi, võib abiks olla soolalahuse perfusioonultraheli või hüstroskoopia. Kompuutertomograafia ei ole emaka fibroidide diagnoosimisel kasulik selle halva selguse ja koe tasapinna visualiseerimise tõttu.
2011. aastal avaldas Rahvusvaheline Sünnitusabi ja Günekoloogia Föderatsioon emakafibroidide klassifikatsioonisüsteemi eesmärgiga kirjeldada paremini fibroidide asukohta emakaõõne ja seroosmembraani pinna suhtes, mitte kasutada vanu termineid submukosaalne, intramuraalne ja subseroosmembraan, võimaldades seeläbi selgemat suhtlust ja ravi planeerimist (lisa lisa tabel S3, mis on koos selle artikli täistekstiga saadaval aadressil NEJM.org). Klassifikatsioonisüsteem on tüüp 0 kuni 8, kus väiksem number näitab, et fibroid asub endomeetriumile lähemal. Segatüüpi emakafibroidid on tähistatud kahe sidekriipsudega eraldatud numbriga. Esimene number näitab fibroidi ja endomeetriumi vahelist suhet ning teine number näitab fibroidi ja seroosmembraani vahelist suhet. See emakafibroidide klassifikatsioonisüsteem aitab arstidel edasist diagnoosimist ja ravi suunata ning parandab suhtlust.
Ravi
Enamiku müoomiga seotud menorraagia raviskeemide puhul on esimene samm menorraagia kontrolli all hoidmine rasestumisvastaste hormoonidega. Menorraagia vähendamiseks saab kasutada ka menstruatsiooni ajal kasutatavaid mittesteroidseid põletikuvastaseid ravimeid ja tranatemotsüklilist hapet, kuid nende ravimite efektiivsuse kohta idiopaatilise menorraagia korral on rohkem tõendeid ning haiguse kliinilistest uuringutest jäetakse tavaliselt välja patsiendid, kellel on hiiglaslikud või submukosaalsed fibroidid. Pika toimeajaga gonadotropiini vabastava hormooni (GnRH) agonistid on heaks kiidetud emaka fibroidide lühiajaliseks preoperatiivseks raviks, mis võib põhjustada amenorröad peaaegu 90%-l patsientidest ja vähendada emaka mahtu 30–60%. Siiski on need ravimid seotud hüpogonadaalsete sümptomite, sealhulgas luukadu ja kuumahoogude suurema esinemissagedusega. Need põhjustavad enamikul patsientidest ka „steroidseid ägenemisi“, mille puhul vabanevad organismis talletatud gonadotropiinid, mis põhjustavad hiljem vererohkeid menstruatsioone, kui östrogeeni tase langeb kiiresti.
Suukaudse GnRH antagonistide kombinatsioonravi kasutamine emakafibroidide ravis on suur edasiminek. Ameerika Ühendriikides heaks kiidetud ravimid ühendavad suukaudsed GnRH antagonistid (elagolix või relugolix) liittabletis või -kapslis östradiooli ja progesterooniga, mis pärsivad kiiresti munasarjade steroidide tootmist (ja ei põhjusta steroidide vallandamist), ning östradiooli ja progesterooni annustega, mis muudavad süsteemse taseme võrreldavaks varajase follikulaarse tasemega. Ühel Euroopa Liidus juba heaks kiidetud ravimil (linzagolix) on kaks annust: annus, mis osaliselt pärsib hüpotalamuse funktsiooni, ja annus, mis täielikult pärsib hüpotalamuse funktsiooni, mis on sarnane elagolixi ja relugoliksi heakskiidetud annustega. Mõlemad ravimid on saadaval preparaadina koos östrogeeni ja progesterooniga või ilma. Patsientidele, kes ei soovi kasutada eksogeenseid gonaadisteroide, võib madala annusega linzagolixi ravimvorm ilma gonaadisteroidide (östrogeeni ja progesterooni) lisamiseta saavutada sama efekti kui suure annusega kombineeritud ravimvorm, mis sisaldab eksogeenseid hormoone. Kombineeritud ravi või ravi, mis osaliselt pärsib hüpotalamuse funktsiooni, võib leevendada sümptomeid, mille toime on võrreldav täisannusega GnRH antagonistide monoteraapiaga, kuid vähemate kõrvaltoimetega. Üks suurte annustega monoteraapia eelis on see, et see suudab emaka suurust efektiivsemalt vähendada, mis sarnaneb GnRH agonistide toimega, kuid millega kaasnevad rohkem hüpogonadaalsed sümptomid.
Kliiniliste uuringute andmed näitavad, et suukaudne GnRH antagonistide kombinatsioon on efektiivne menorraagia (50–75% vähenemine), valu (40–50% vähenemine) ja emaka suurenemisega seotud sümptomite vähendamisel, vähendades samal ajal veidi emaka mahtu (emaka mahu vähenemine ligikaudu 10%) ja tekitades vähem kõrvaltoimeid (<20% osalejatest kogesid kuumahooge, peavalu ja iiveldust). Suukaudse GnRH antagonistide kombinatsioonravi efektiivsus ei sõltunud müomatoosi ulatusest (fibroidide suurus, arv või asukoht), adenomüoosi keerukusest ega muudest kirurgilist ravi piiravatest teguritest. Suukaudne GnRH antagonistide kombinatsioon on Ameerika Ühendriikides praegu heaks kiidetud 24 kuuks ja Euroopa Liidus määramata ajaks kasutamiseks. Siiski ei ole neil ravimitel näidatud rasestumisvastast toimet, mis piirab paljude inimeste pikaajalist kasutamist. Relugolix'i kombinatsioonravi rasestumisvastast toimet hindavad kliinilised uuringud on käimas (registreerimisnumber NCT04756037 aadressil ClinicalTrials.gov).
Paljudes riikides on selektiivsed progesterooni retseptori modulaatorid ravimrežiimil. Kuid haruldase, kuid tõsise maksatoksilisuse mure on piiranud selliste ravimite aktsepteerimist ja kättesaadavust. Ameerika Ühendriikides ei ole emakafibroidide raviks heaks kiidetud ühtegi selektiivset progesterooni retseptori modulaatorit.
Hüsterektoomia
Kuigi hüsterektoomiat on ajalooliselt peetud emakamüoomide radikaalseks raviks, viitavad uued andmed sobivate alternatiivsete ravimeetodite tulemuste kohta sellele, et need võivad kontrollitud aja jooksul olla hüsterektoomiaga mitmes mõttes sarnased. Hüsterektoomia puudusteks võrreldes teiste alternatiivsete ravimeetoditega on perioperatiivsed riskid ja salpingektoomia (kui see on protseduuri osa). Enne sajandivahetust oli mõlema munasarja eemaldamine koos hüsterektoomiaga tavaline protseduur ning 2000. aastate alguse suured kohortuuringud näitasid, et mõlema munasarja eemaldamine oli seotud suurenenud surma, südame-veresoonkonna haiguste, dementsuse ja muude haiguste riskiga võrreldes hüsterektoomia tegemise ja munasarjade säilitamisega. Sellest ajast alates on salpingektoomia kirurgiline määr vähenenud, samas kui hüsterektoomia kirurgiline määr mitte.
Mitmed uuringud on näidanud, et isegi kui mõlemad munasarjad säilitatakse, suureneb pärast hüsterektoomiat oluliselt südame-veresoonkonna haiguste, ärevuse, depressiooni ja surma risk. Suurimas riskis on patsiendid, kes hüsterektoomia ajal on ≤35-aastased. Nende patsientide seas oli südame isheemiatõve (pärast segavate tegurite arvessevõtmist) ja südame paispuudulikkuse risk 2,5 korda suurem naistel, kellele tehti hüsterektoomia, ja 4,6 korda suurem naistel, kellele hüsterektoomiat ei tehtud 22-aastase jälgimisperioodi jooksul. Naistel, kellele tehti hüsterektoomia enne 40. eluaastat ja kellel munasarjad säilitati, oli 8–29 protsenti suurem suremise tõenäosus kui naistel, kellel hüsterektoomiat ei tehtud. Hüsterektoomia läbinud patsientidel oli aga rohkem kaasuvaid haigusi, nagu rasvumine, hüperlipideemia või operatsiooni anamnees, kui naistel, kellel hüsterektoomiat ei tehtud, ja kuna need uuringud olid vaatluslikud, ei saanud põhjuslikku seost kinnitada. Kuigi uuringutes on neid loomupäraseid riske kontrollitud, võib siiski esineda mõõtmata segavaid tegureid. Neid riske tuleks selgitada patsientidele, kes kaaluvad hüsterektoomiat, kuna paljudel emakamüoomidega patsientidel on vähem invasiivsed alternatiivid.
Praegu puuduvad emakafibroidide primaarsed ega sekundaarsed ennetusstrateegiad. Epidemioloogilised uuringud on leidnud mitmeid tegureid, mis on seotud emakafibroidide vähenenud riskiga, sealhulgas: rohkem puu- ja köögiviljade ning vähem punase liha söömine; regulaarne treening; kehakaalu kontrollimine; normaalne D-vitamiini tase; edukas elussünnitus; suukaudsete rasestumisvastaste vahendite kasutamine; ja pika toimeajaga progesteroonipreparaadid. Selleks, et teha kindlaks, kas nende tegurite muutmine võib riski vähendada, on vaja randomiseeritud kontrollitud uuringuid. Lõpuks viitab uuring sellele, et stress ja rassism võivad mängida rolli emakafibroididega seotud tervisealase ebaõigluse tekkimises.
Postituse aeg: 09.11.2024