Segatüüpi hüperlipideemiat iseloomustab madala tihedusega lipoproteiinide (LDL) ja triglütseriidirikaste lipoproteiinide kõrgenenud plasmakontsentratsioon, mis suurendab aterosklerootilise kardiovaskulaarse haiguse riski selles patsientide populatsioonis.
ANGPTL3 inhibeerib lipoproteiini lipaasi ja endosepiaasi, samuti triglütseriidirikaste lipoproteiinide omastamist maksas. ANGPTL3 inaktiveeritud variandi kandjatel oli madalam triglütseriidide, LDL-kolesterooli, kõrge tihedusega lipoproteiini (HDL) kolesterooli ja mitte-HDL-kolesterooli tase, samuti madalam aterosklerootilise kardiovaskulaarse haiguse risk. Zodasiraan on väike interfereeriv RNA (RNAi) ravim, mis on suunatud ANGPTL3 ekspressioonile maksas.
Segatüüpi hüperlipideemia viitab madala tihedusega lipoproteiini kolesterooli (LDL-C) ja triglütseriidirikaste lipoproteiinide kõrgenenud tasemele. Triglütseriidirikkad lipoproteiinid (sealhulgas külomikronid, väga madala tihedusega lipoproteiinid (VLDL) ja jääkkolesterool) mängivad olulist rolli aterosklerootilise haiguse tekkes. Segatüüpi hüperlipideemiale puudub efektiivne ravi.
On teada, et Bates vähendab triglütseriidide (TG) taset, kuid see langus on piiratud. Samal ajal ei ole TG taset langetavatel ravimitel, sealhulgas Batesil (näiteks eikosapentaeenäädikhappel jne), olulist mõju kõrgenenud jääkkolesterooli tasemest tingitud aterosklerootilise haiguse riskile. Lisaks on varasemad statiine juba võtvate patsientide uuringud näidanud, et TG taset langetavate ravimite kombinatsioon ei vähenda kardiovaskulaarsete sündmuste riski. Need tegurid muudavad segatüüpi hüperlipideemia ravi väga keeruliseks.
ANGPTL3 (angiopoietiinilaadne valk 3) reguleerib lipiidide ja lipoproteiinide metabolismi, sealhulgas TG ja mitte-kõrge tihedusega lipoproteiini kolesterooli (HDL-C), pärssides pöörduvalt lipoproteiini lipaasi, endosepiaasi ja madala tihedusega lipoproteiini (LDL) retseptorist sõltuvat maksa lipoproteiinide omastamist. On leitud, et ANGPTL3 inaktiveerimisvariant viib lipoproteiini lipaasi ja endosepiaasi aktiivsuse suurenemiseni, mis omakorda viib enamikul juhtudel madala plasma lipoproteiinide tasemeni. Nende hulka kuuluvad triglütseriidirikkad lipoproteiinid (st külomikronid, jääkkolesterool, VLDL, keskmise tihedusega lipoproteiin [IDL]), LDL, kõrge tihedusega lipoproteiin (HDL), lipoproteiin (a) ja nende kolesterooli komponendid. Heterosügootsetel inimestel, kes kannavad seda varianti, on aterosklerootilise haiguse risk ligikaudu 40% väiksem ja kliinilist fenotüüpi ei ole leitud. ANGPTL3 ekspresseerub maksas ja selle mRNA-le suunatud geeni vaigistamise teraapiad, mida tuntakse väikeste interfereerivate RNA (siRNA) ravimitena, on paljulubav hübriidravi hüperlipideemia raviks.
12. septembril 2024 avaldas New England Journal of Medicine (NEJM) ARCHES 2 uuringu, mis kinnitas, et siRNA ravim zodasiraan vähendas oluliselt triglütseriidide taset segatüüpi hüperlipideemiaga patsientidel [1]. ARCHES-2 on topeltpime, platseebokontrolliga, annusvahemiku uurimise faasi 2b uuring. Uuringusse kaasati kokku 204 segatüüpi hüperlipideemiaga patsienti (tühja kõhuga triglütseriidide tase 150–499 mg/dl, LDL-kolesterooli tase ≥70 mg/dl või mitte-HDL-kolesterooli tase ≥100 mg/dl). Nad jagati zodasiraani 50 mg gruppi, 100 mg gruppi, 200 mg gruppi ja platseebokontrollgruppi. Patsiendid said subkutaanseid süste 1. ja 12. nädalal ning said järelprofülaktikat kuni 36. nädalani.
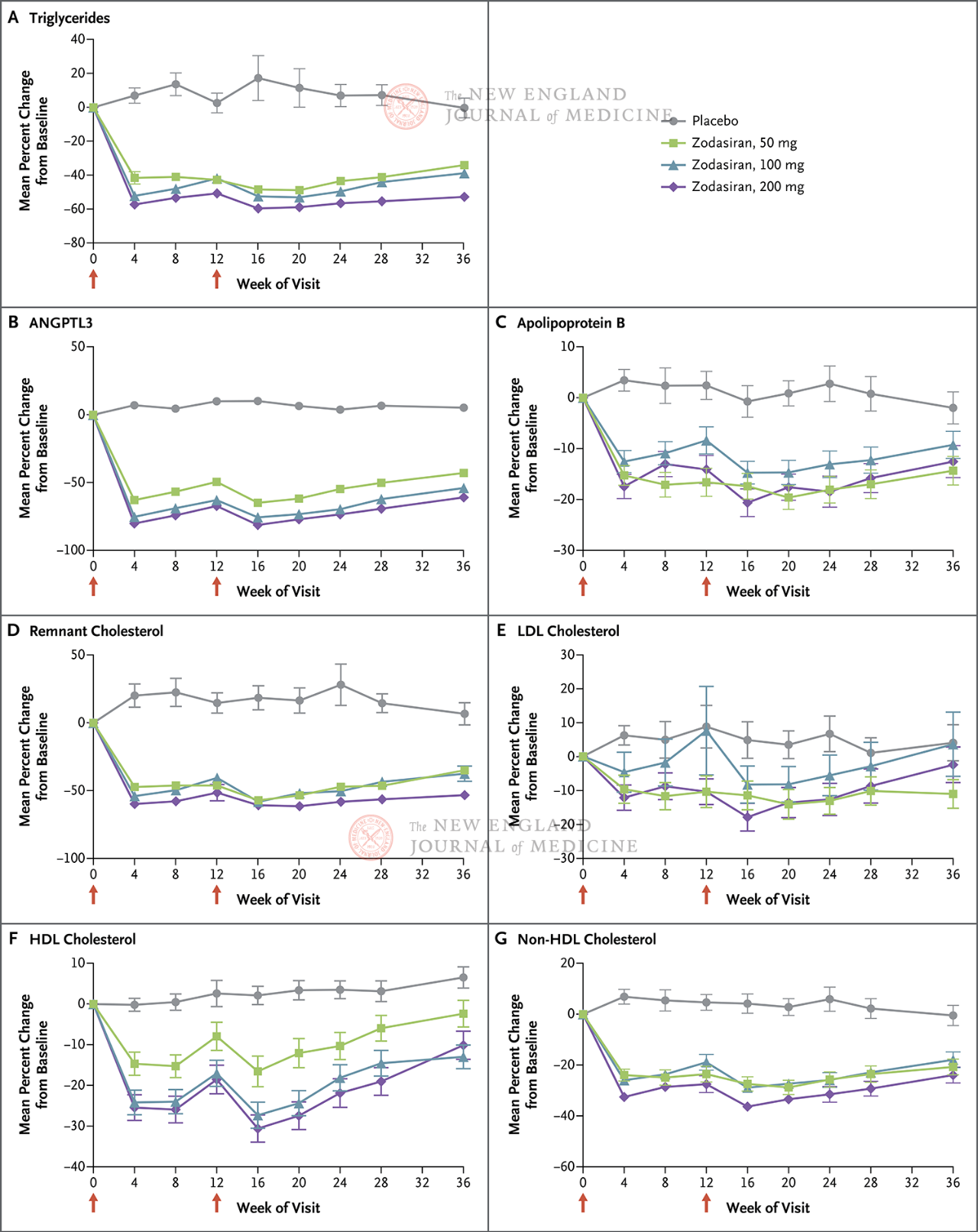
Esmane tulemusnäitaja oli triglütseriidide (TG) protsentuaalne muutus algtasemest 24. nädalani. Uuringus leiti, et 24. nädalaks oli zodasiraani rühmas triglütseriidide (TG) tase annusest sõltuvalt oluliselt vähenenud (TG tase igas annuserühmas langes vastavalt 51, 57 ja 63 protsendipunkti võrreldes platseeborühmaga) (P<0,001 kõigi võrdluste puhul). ANGPTL3 tase langes samuti vastavalt 54, 70 ja 74 protsendipunkti võrra. Mitte-HDL-kolesterooli tase langes 29, 29 ja 36 protsendipunkti võrra, apolipoproteiin B tase langes 19, 15 ja 22 protsendipunkti võrra ning LDL-kolesterooli tase langes vastavalt 16, 14 ja 20 protsendipunkti võrra ning need tulemused püsisid kuni 36. nädalani. 24. nädalal zodasiraani...
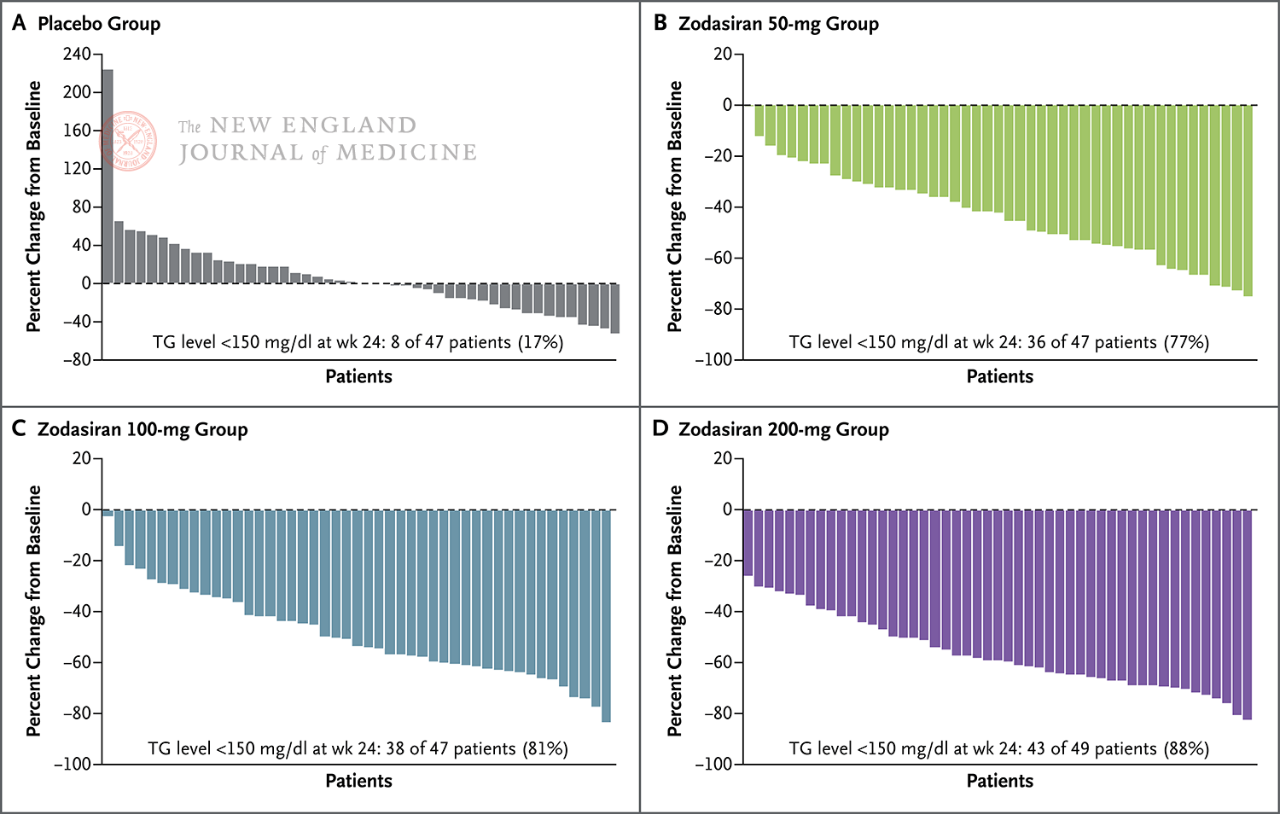
88%-l patsientidest 200 mg rühmas oli tühja kõhuga TG langenud normivahemikku.
Punased nooled 1. ja 12. päeval näitavad zodasirani või platseebo manustamist.
Tühja kõhuga TG tase langes 24. nädalaks normaalsele tasemele (150
mg/dl või vähem)
Iga sammas esindab ühte patsienti.
Uuringus täheldati ka, et zotasiraan oli ohutu kõigis annusgruppides, kusjuures ainult 2 patsienti katkestas uuringu kõrvaltoimete tõttu (1 platseebogrupis ja 1 100 mg zotasiraani grupis). Kõik tõsised kõrvaltoimed zotasiraani grupis taandusid uuringu lõpuks ja platseebogrupis oli üks surmajuhtum. Ainus murettekitav kõrvaltoime oli HBA1c suurenemine 200 mg zotasiraani grupis võrreldes platseeboga (keskmine muutus algtasemest 24. nädalani [±SD] 0,38±0,66% vs -0,03±0,88% olemasoleva diabeediga patsientidel). Diabeedita patsiente oli 0,12±0,19% vs -0,03±0,19%).
Täpsemalt öeldes raviti peaaegu kõiki uuringus osalenud patsiente (96%) statiinidega (kellest 37% olid suurtes annustes statiinid), 1% raviti proproteiini konverteeriva ensüümi subtilüsiin 9 inhibiitoriga (PCSK9i) ja 21% raviti fibraatidega. Seega saavutati zodasirani lisamisega praegusele tavapärasele raviskeemile siiski märkimisväärne lipiidide taset langetav toime, mis pakub tulevikus uut raviskeemi segatüüpi hüperlipideemia raviks.
24. nädalal vähendas uuringus manustatud zotasiraani maksimaalne annus 200 mg jääkkolesterooli taset platseeboga võrreldes 34,4 mg/dl võrra. Praeguste mudelite põhjal eeldatakse, et see vähenemine vähendab peamisi südamega seotud kõrvaltoimeid 20 protsenti. Zodasiraanil on potentsiaali kasutada monoteraapiana kõigi lipoproteiini komponentide puhul, et vähendada patsientidel kardiovaskulaarsete sündmuste riski. Seetõttu on vaja täiendavaid uuringuid, et teha kindlaks selle ravimi potentsiaal aterosklerootilise haiguse riski vähendamisel.
NEJM-is samaaegselt avaldatud 2b faasi topeltpimedas, randomiseeritud, platseebokontrolliga MUIR-uuringus kasutati segatüüpi hüperlipideemia [2] raviks teist siRNA-ravimit, plozasiraani. Plozasiraan on loodud vähendama maksas apolipoproteiin C3 (APOC3) kodeeriva geeni APOC3 ekspressiooni, mis on TG metabolismi regulaator, vähendades seeläbi TG ja jääkkolesterooli taset. Uuringus täheldatud TG ja jääkkolesterooli taseme langus oli sarnane ARCHES-2 uuringus täheldatuga. Seetõttu oletatakse, et segatüüpi hüperlipideemiaga patsientidel on kahel ravimil sarnane toime triglütseriididerikka lipoproteiini ja jääkkolesterooli taseme vähendamisel.
Kahe siRNA uuringu tulemused näitavad, et tegemist on väga paljutõotava ravimiklassiga, mis pakub uusi võimalusi segatüüpi hüperlipideemia raviks ja parandab patsientide kardiovaskulaarseid tulemusi.
Postituse aeg: 15. september 2024